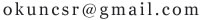Cu+2H2SO4(浓)=CuSO4+SO2↑+H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
因此,体现这些酸的酸性的不是氢离子,而是高价非金属元素
此外,活泼金属与浓度很稀的硝酸有时也会产生NH4NO3,N2
学到氧化还原反应的时候(高中)就知道了。
而且浓硝酸会使某些金属钝化
为什么金属和浓硫酸,硝酸反应不生成氢气
因为浓硫酸和硝酸都具有强氧化性,普通的酸具有氧化性体现在氢离子得电子生成氢气的能力上,而所谓强氧化性就是说浓硫酸和硝酸酸根得电子的能力比氢离子还要强,在反应中,它们的酸根得电子生成SO2,NO(稀硝酸),NO2(浓硝酸),而氢离子因为抢不到电子,就无法生成氢气。
为什么金属和浓硫酸,硝酸反应不生成氢气
强氧化性酸和金属不发生还原反应,而是具有金属性(可理解为还原性)的金属失电子,化合价升高,强氧化性酸中的高价元素(S,N)得电子,化合价降低,一般放出含有这种元素的氧化物(气体),如:Cu+2H2SO4(浓)=CuSO4+SO2↑+H2O 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O Cu+4HNO3(浓)=Cu(N...
为什么金属和浓硫酸,硝酸反应不生成氢气
强氧化性酸和金属不发生还原反应,而是具有金属性(可理解为还原性)的金属失电子,化合价升高,强氧化性酸中的高价元素(S,N)得电子,化合价降低,一般放出含有这种元素的氧化物(气体),如:Cu+2H2SO4(浓)=CuSO4+SO2↑+H2O 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O Cu+4HNO3(浓)=Cu(N...
为什么硝酸和浓硫酸不能与金属反应产生氢气
那是因为硝酸和浓硫酸与金属反应,表现出氧化性的离子为NO3-和SO42-而不是氢离子,那么相应的还原产物就不可能是氢气,所以不能与金属反应生成氢气。根据金属活动顺序表K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au可从定性和定量两方面进行归纳总结:一、定性方面 ① 排在金属...
硝酸和浓硫酸和金属反应为什么不生成气体
是不生成氢气,不是“不生成气体”。因为浓硫酸中,S元素表现强氧化性,S得电子生成SO2。(而不会由H原子得电子,所以不能生成H2)方程式: Mg+2H2SO4=MgSO4+SO2+2H2O 同理,浓硝酸中N原子表现强氧化性,N原子得电子生成NO2.方程式:Mg+4HNO3=Mg(NO3)2+2H2O+2NO2 ...
浓硫酸,硝酸与金属反应为什么不能生成氢气
浓度太高。浓硫酸能使铁、铝等金属钝化。主要原因是硫酸分子与这些金属原子化合,生成致密的氧化物薄膜,防止氢离子或硫酸分子继续与金属反应。浓硫酸,俗称坏水,化学分子式为H₂SO₄,是一种具有高腐蚀性的强矿物酸。浓硫酸指质量分数大于或等于70%的硫酸溶液。浓硫酸在浓度高时具有强氧化...
铁与浓硝酸或者浓硫酸反应为什么不产生氢气?
即它俩的氧化性比H+强,所以作为还原剂的金属单质失去的电子会优先被N和S得到。这样H+得不到电子自然就无法生成H2了。哦对了,对于铁来说铁单质在浓硝酸和浓硫酸中会钝化,表面生成一层致密的氧化膜,阻止了铁和酸继续反应,所以不会产生H2。
硝酸和金属反应不产生氢气?为什么?
因为硝酸是强氧化性酸,强氧化性酸和金属反应不会生成氢气。稀硝酸和金属反应生成一氧化氮,浓硝酸和金属反应生成二氧化氮,不会有氢气生成的。同理,浓硫酸也是强氧化性酸,和金属反应生成二氧化硫,而不是氢气。
硝酸为什么与金属反应不会产生氢气
硝酸与金属反应之所以不会产生氢气,是因为硝酸是一种强氧化剂、硝酸根离子具有比氢离子更大的氧化性,所以氢不参与氧化反应,从而,也就不产生氢气了。硝酸是一种具有强氧化性、腐蚀性的强酸,属于一元无机强酸,是六大无机强酸之一,也是一种重要的化工原料。在工业上可用于制化肥、农药、炸药、染料、...
为什么金属与浓硫酸,硝酸反应通常不生成氢气?
简单的说,可以这么理解:(氢活动性之前的)金属 与普通酸反应,生成氢气 实际上也是一个 氧化还原反应,(氢离子氧化性不强,一般很少说它的氧化性),但是在硝酸中,硝酸根离子的氧化性远远大于氢离子,所以一般金属会先与硝酸根离子起反应。